L’acalasia è un disordine motorio esofageo raro. Si caratterizza per l’alterato rilasciamento dello sfintere esofageo inferiore (LES) e per la mancata peristalsi (il complesso delle contrazioni anulari del tubo digerente, che permettono il transito del cibo) a livello del corpo esofageo.
La sintomatologia clinica è caratterizzata dalla presenza di:
- disfagia (disturbi della deglutizione);
- rigurgito di cibo indigerito;
- dolore toracico;
- perdita di peso;
- manifestazioni respiratorie (tosse notturna, aspirazioni ricorrenti di materiale alimentare fino ad arrivare a quadri di polmonite ab ingestis).
L’acalasia è il risultato della scomparsa dei neuroni del plesso mioenterico, che coordinano la peristalsi esofagea e il rilasciamento del LES (sfintere esofageo inferiore).
La maggior parte delle forme di acalasia sono a genesi idiopatica (senza una causa nota o dimostrabile) e si presentano per lo più in forma sporadica. Tuttavia, all’esordio dei sintomi, è importante differenziare l’acalasia vera da altre condizioni di “pseudo-acalasia”, quali:
- la Malattia di Chagas (causata dalla degenerazione del plesso mioenterico provocata dall’infezione del parassita Trypanosoma cruzi);
- oppure condizioni neoplastiche, che possono causare i sintomi o per infiltrazione diretta della giunzione gastroesofagea o per via paraneoplastica (carcinoma polmonare a piccole cellule, SCLC).
L’acalasia è un disordine raro, con un’incidenza annuale stimata di circa 1,07-2,2 per 100.000 individui e una prevalenza di circa 10-15,7 su 100.000 soggetti. Non c’è predominanza di genere né di etnia.
Sebbene possa presentarsi a qualsiasi età, è raro prima della seconda decade di vita. L’incidenza aumenta, invece, con l’età e raggiunge il picco nella settima decade (17/100.000 casi per anno). Un altro picco, di minore incidenza, si raggiunge tra i 20 e i 40 anni. In genere, l’età media alla diagnosi è superiore ai 50 anni.
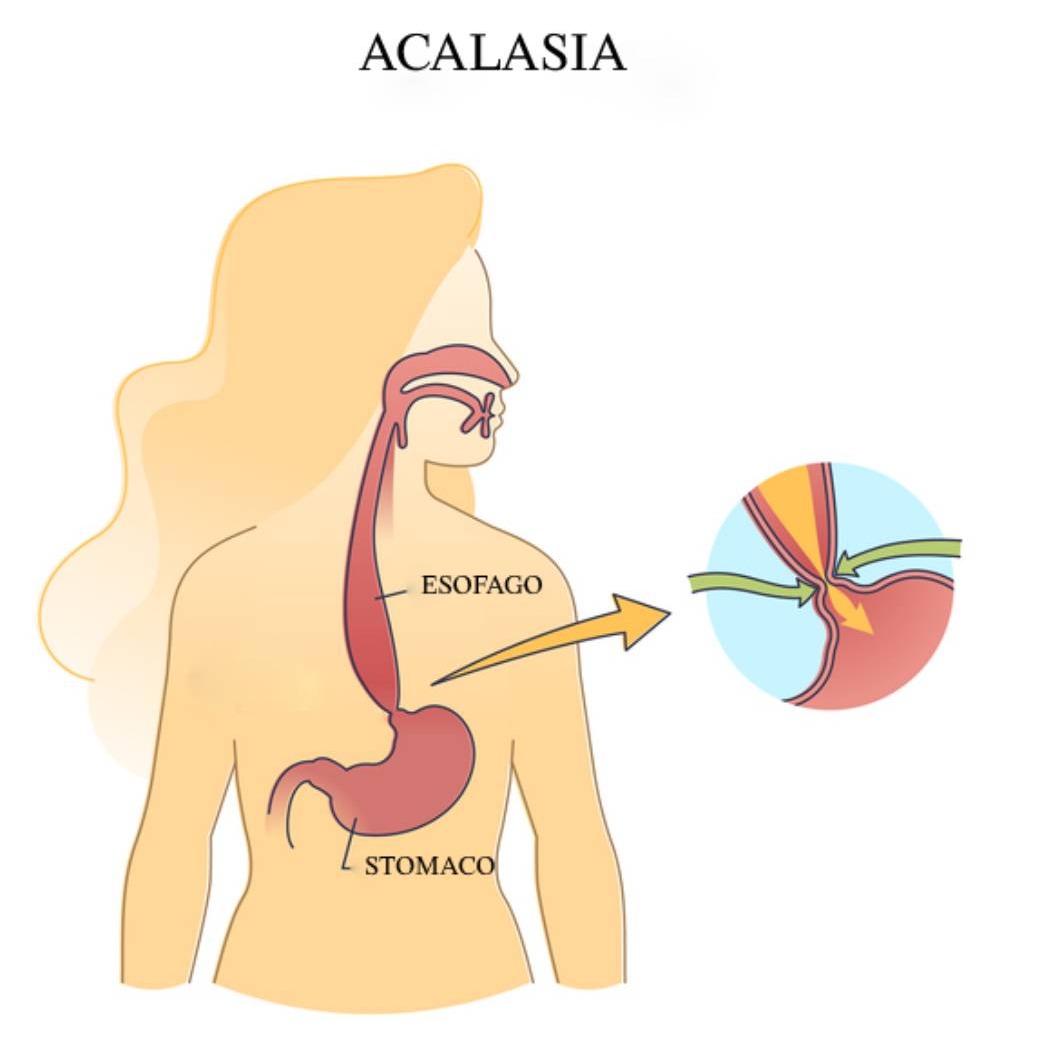
 Cause
Cause
In condizioni normali, il passaggio del bolo in esofago è consentito dalla presenza di onde peristaltiche coordinate e dal rilasciamento del LES, entrambi coordinati dai neuroni del plesso mioenterico. Nell’acalasia, i neuroni del plessomioenterico, ed in particolare quelli inibitori contenenti ossido nitrico (NO) e peptide vasoattivo intestinale (VIP), appaiono ridotti numericamente o assenti, con il conseguente:- mancato rilasciamento del LES (sfintere esofageo inferiore);
- l’alterata peristalsi;
- l’anomala funzione esofagea.
Altri studi, inoltre, hanno dimostrato la presenza di anticorpi circolanti diretti contro i neuroni mioenterici nel siero di pazienti acalasici, specialmente in coloro che presentavano gli alleli HLA DQA1*0103 e DQB1*0603. Si è ipotizzato che la presenza di una risposta immune aberrante, scatenata dall’esposizione ad antigeni sconosciuti, possa avere un ruolo patogenetico fondamentale. Alcuni virus, tra cui il Virus Herpes Simplex 1 (HSV-1) ed il Papillomavirus umano, sono stati proposti quali potenziali antigeni.
Allo stato attuale, l’ipotesi più accreditata è quella di un disordine a genesi multifattoriale, caratterizzato da un’alterata risposta immune cellulo-mediata rivolta contro i neuroni del plesso mioenterico a livello esofageo e scatenata, in soggetti geneticamente predisposti, da fattori “trigger” (scatenante).
 Sintomi
Sintomi
La sintomatologia clinica si caratterizza per:
- la presenza di disfagia per solidi e liquidi (>90%);
- rigurgito di cibo indigerito (76-91%);
- manifestazioni respiratorie (tosse notturna [30%] e aspirazione [8%]);
- calo ponderale (35-91%);
- dolore toracico (25-64%);
- pirosi (18-52%), che talvolta porta all'erronea diagnosi di Malattia da Reflusso Gastroesofageo.
La tosse notturna è più frequente in pazienti che presentano una severa stasi di cibo e secrezioni a livello esofageo.
 Diagnosi
Diagnosi
La mancanza di sintomi specifici o patognomonici causa spesso un notevole ritardo diagnostico (fino a 5 anni).
Molto utilizzato, per la valutazione del quadro clinico dell'Acalasia, è l'Eckardt score, che assegna un punteggio da 0 a 3 a:
- disfagia;
- dolore retrosternale;
- rigurgito;
- al calo ponderale.
Il punteggio totale va da 0 a 12. Oltre ad essere il più diffuso score per valutare lo stato di attività della patologia, è anche predittivo della risposta al trattamento, che si considera andato a buon fine laddove il punteggio sia inferiore a 3.
Nell'iter diagnostico del paziente con sospetto di acalasia, è fondamentale l'esecuzione della esofagogastroduodenoscopia (EGDS), che può evidenziare dilatazione del viscere, ritenzione di residui alimentari e saliva, oltre che da una resistenza, quando l'endoscopio cerca di attraversare la giunzione esofago-gastrica, seguita da un improvviso passaggio in cavità gastrica, definita come "segno dello scatto". L'aspetto della mucosa può essere normale o presentare segni di esofagite.
L'esecuzione di biopsie, durante l'esame endoscopico, è importante per escludere altre condizioni quali l'esofagite eosinofila. L'endoscopia è inoltre un esame fondamentale per escludere un'occlusione meccanica su base neoplastica, quindi per escludere una pseudo-acalasia.
Il gold standard per la diagnosi di Acalasia è la manometria esofagea ad alta risoluzione (HRM). Questa metodica consente di studiare la motilità dell'esofago, introducendo al suo interno un catetere costituito da micro-trasduttori allo stato solido e da 36 sensori distanziati di 1 cm, che permettono di misurare la dinamica pressoria del viscere. Specifici algoritmi vanno poi a tramutare i dati ricavati dai sensori, in una scala colorimetrica topografica, dove, a una certa pressione, corrisponde un colore. Il protocollo standard della Chicago Classification 4.0, per l'esecuzione della manometria ad alta risoluzione, prevede lo studio della peristalsi indotta dalla deglutizione, studiando il paziente sia in posizione supina che eretta. Il catetere viene inserito nella narice del paziente, previa apposizione di un gel anestetico. Se il posizionamento è avvenuto correttamente, si potranno visualizzare lo sfintere esofageo superiore (UES), quello inferiore (LES) ed il diaframma crurale (CD).
Dal punto di vista manometrico, possiamo distinguere tre tipi di Acalasia:
- nell'Acalasia di tipo I, si riscontra un IRP elevato associato all'assenza di contrattilità, ovvero il 100% della peristalsi è fallita (DCI <100 mmHg-s-cm);
- nell'Acalasia di tipo II, l'IRP elevato si associa all'assenza di contrattilità e a una pressurizzazione panesofagea, almeno nel 20% delle deglutizioni;
- nell'Acalasia di tipo III, si riscontrano IRP elevato, assenza di peristalsi in associazione a spasmo esofageo, ovvero una contrazione prematura (DL < 4.5 s) in almeno il 20% delle deglutizioni.
La classificazione dell'Acalasia nei tre sottotipi è importante non solo ai fini diagnostici, ma ha anche una valenza prognostica. È stato dimostrato come pazienti affetti da Acalasia di tipo II e di tipo I rispondano meglio alla terapia, in particolar modo alla dilatazione pneumatica ed alla miotomia sec. Heller, rispetto al tipo III.
 Cure e Trattamenti
Cure e Trattamenti
Ad oggi, non esiste alcun trattamento in grado di permettere il recupero della peristalsi esofagea. La terapia è palliativa con lo scopo di ridurre i sintomi, favorire lo svuotamento dell'esofago, prevenire la dilatazione dell'organo.
I trattamenti disponibili sono:
- la terapia farmacologica orale. Il trattamento farmacologico prevede la somministrazione di calcio antagonisti (Nifedipina10- 30 mg prima dei pasti) o nitrati (Isosorbide dinitrato 5-10 mg prima dei pasti). La loro efficacia, nel rilassare lo sfintere esofageo inferiore, va dal 47% al 64%, portando ad un lieve miglioramento della disfagia. La principale limitazione è rappresentata dalla breve durata d'azione dei farmaci, che dovranno essere somministrati più volte al giorno, esponendo il paziente a numerosi effetti collaterali, come cefalea, ipotensione e edemi agli arti inferiori. La terapia farmacologica è la meno efficace e va riservata a pazienti non candidabili alle altre opzioni terapeutiche, oppure come “bridge therapy” verso un altro trattamento;
- l'iniezione endoscopica di tossina botulinica. Altro importante presidio terapeutico è l'iniezione endoscopica di tossina botulinica (BT). L'efficacia del trattamento nel rilassamento del LES è data dal clivaggio della proteina SNAP-25, fondamentale per la fusione della vescicola presinaptica, contenente acetilcolina, con la membrana plasmatica. Il farmaco blocca quindi il rilascio del neurotrasmettitore nello spazio sinaptico, bloccando la trasmissione eccitatoria che, nel paziente affetto da Acalasia, non è efficacemente controbilanciata da quella inibitoria. La dose di tossina botulinica raccomandata è di 100 U, distribuita equamente all'interno dei quattro quadranti dello sfintere, prossimalmente alla giunzione squamo-colonnare. Gli effetti collaterali sono scarsi e il più frequentemente lamentato dai pazienti è un dolore toracico transitorio. L'efficacia del trattamento si riduce però nel tempo, con necessità di ripetere il trattamento nel 46.6% dei pazienti. L'iniezione di tossina botulinica è quindi una terapia di prima linea solo nei pazienti non candidabili a miotomia, data la loro maggiore efficacia rispetto alla farmacoterapia orale e gli scarsi effetti collaterali;
- la dilatazione endoscopica. La dilatazione pneumatica (PD) è un'altra valida opzione nel trattamento dell'Acalasia. Questa tecnica prevede il passaggio di dilatatori attraverso lo sfintere esofageo inferiore, in modo da sfiancare la muscolatura e favorire il passaggio del bolo. Anche in questo caso, l'efficacia non è ottimale nel lungo termine e 1/3 dei pazienti recidiva, infatti, entro i successivi 4-6 anni. La principale complicanza del trattamento è la perforazione del viscere, che si presenta nell' 1,9% dei pazienti. Altro comune effetto collaterale è la comparsa di reflusso gastroesofageo, che si dimostra però responsivo agli IPP;
- la miotomia secondo Heller. La miotomia è stato il primo trattamento chirurgico ad essere effettuato per l'Acalasia, eseguito per la prima volta da Ernst Heller nel 1913. La procedura consiste nell'eseguire un taglio longitudinale delle fibre dello sfintere esofageo inferiore, vengono quindi separate le fibre muscolari dello strato circolare senza andare ad intaccare la mucosa. L'esito è da buono ad eccellente nel 60% - 90% dei pazienti. L'efficacia della miotomia si riduce con il passare del tempo, passando dall'89% di successo nel follow up a sei mesi al 57% a 6 anni. Anche per il trattamento chirurgico, inoltre, l'Acalasia di tipo II risulta essere un fattore prognostico positivo, avendo un outcome migliore del tipo I e del tipo III. La miotomia secondo Heller è un trattamento che può essere proposto in prima linea ai pazienti candidabili al trattamento chirurgico. La maggior parte degli autori ritiene inoltre che sia superiore alla dilatazione pneumatica per quanto riguarda la remissione clinica, il tasso di recidiva e la sicurezza;
- la miotomia endoscopica transorale (POEM). Il trattamento più recente proposto per l'Acalasia è la miotomia esofagea transorale (POEM), con la quale si pratica la miotomia per via endoscopica. La percentuale di successo, definita da un miglioramento nei sintomi e dall'assenza di necessità di ulteriori trattamenti, è risultata maggiore del 90%, anche se sono necessari ulteriori studi a lungo termine. La principale complicanza è l'insorgenza di malattia da reflusso gastroesofageo.
Bibliografia
- Achalasia. Islam S. Semin Pediatr Surg. 2017 Apr;26(2):116-120. doi: 10.1053/j.sempedsurg.2017.02.001. Epub 2017 Feb 3. PMID: 28550869.
- Achalasia. Walzer N, Hirano I. Gastroenterol Clin North Am. 2008 Dec;37(4):807-25, viii. doi: 10.1016/j.gtc.2008.09.002. PMID: 19028319.
- Achalasia. New concepts. Ruiz de León San Juan A, Pérez de la Serna Y Bueno J. Med Clin (Barc). 2017 May 23;148(10):453-455. doi: 10.1016/j.medcli.2016.12.009. Epub 2017 Jan 29.
- PMID: 28143652.
- Pathophysiology of achalasia. Hirano I. Curr Gastroenterol Rep. 1999 Jun;1(3):198-202. doi: 10.1007/s11894-999-0034-2. PMID: 10980949 Review.
- Achalasia: a comprehensive review. St Peter SD, Swain JM. Surg Laparosc Endosc Percutan Tech. 2003 Aug;13(4):227-40. doi: 10.1097/00129689-200308000-00002. PMID: 12960784.
- Esophageal achalasia: current diagnosis and treatment. Schlottmann F, Patti MG. Expert Rev Gastroenterol Hepatol. 2018 Jul;12(7):711-721. doi: 10.1080/17474124.2018.1481748. Epub 2018 Jun 8. PMID: 29804476.
L'informazione presente nel sito deve servire a migliorare, e non a sostituire, il rapporto medico-paziente. In caso di disturbi e/o malattie rivolgiti al tuo medico di base o ad uno specialista.
Cerca i migliori specialisti che si occupano di Acalasia- Chirurgo Generale a Roma
- Chirurgo Generale a Milano
- Chirurgo Generale a Monza e Brianza
- Chirurgo Generale a Brescia
Revisione Scientifica

Trova il Medico più adatto alle tue esigenze.