Quanti tumori della pelle esistono?
A carico della cute possono insorgere numerose lesioni con caratteristiche cliniche, patologiche ed evolutive diverse. Alcune lesioni della cute e delle mucose hanno significato di precancerosi, potendo andare incontro a trasformazione maligna. Ad esse appartengono la cheratosi cheratosi attinica, il corno cutaneo, la malattia di Bowen, l’eritroplasia di Queyrat, la leucoplachia e il morbo di Paget.
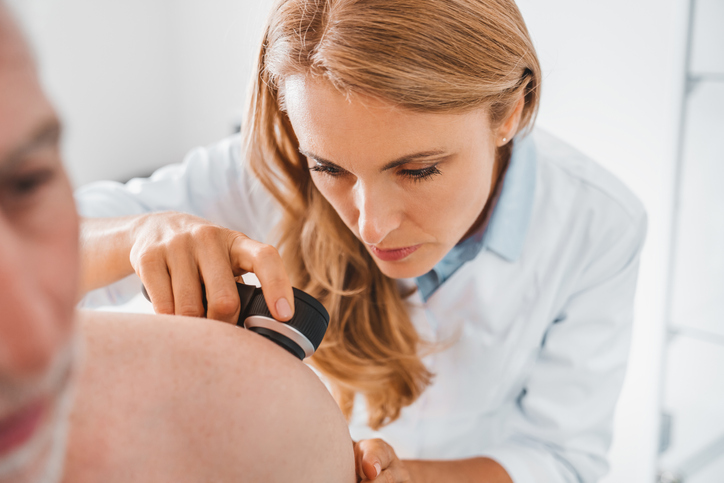
Col termine di tumori cutanei non melanoma, generalmente, si fa riferimento ai carcinomi squamocellulare e basocellulare. Questi, tuttavia, possono essere meglio denominati col termine di carcinomi cheratinocitici, dovendo annoverare nei tumori cutanei non-melanoma anche i sarcomi e i tumori annessiali, che differiscono notevolmente dai carcinomi (squamo- o basocellulari) sia per istogenesi che per caratteristiche cliniche ed epidemiologiche.
Infine, una particolare neoplasia cutanea, è il carcinoma a cellule di Merkel, di derivazione neuroendocrina.poiché esistono altri tumori cutanei diversi dal melanoma, quali i sarcomi e i tumori annessiali, che differiscono notevolmente dai carcinomi a cellule squamose o basali sia per quanto riguarda la cellula di origine che per le caratteristiche cliniche ed epidemiologiche. Infine, un tipo particolare di tumore cutaneo, che origina dalle cellule neuroendocrine intraepiteliali, è il carcinoma a cellule di Merkel.
Per precancerosi si intendono lesioni o quadri patologici cutanei predisponenti a neoplasie di origine prevalentemente epiteliale. Infatti accanto alla cheratosi attinica ed alla leucoplachia, anche radiodermiti ed ulcere croniche cutanee sono da considerarsi potenzialmente cancerogene. Patologie quali lo xeroderma pigmentoso, l’epidermoplasia verruciforme ed il lichen scleroatrofico, vanno tenute sotto stretta sorveglianza in quanto, nella loro evoluzione clinica, possono dare origine a carcinomi spinocellulari.
Cheratosi attinica
Chi è più colpito?
- Incidenza: molto comune con un progressivo aumento di incidenza in europa;
- sesso: più frequente nel sesso maschile;
- età: in genere compare dopo i 40 anni;
- etnia: più frequente nei soggetti con fototipo chiaro (i, ii, iii), molto rari nelle persone nere;
- sede anatomica; sedi fotoesposte, soprattutto il dorso delle mani, la fronte, il naso e il cuoio capelluto nei soggetti calvi. La cheilite attinica è una cheratosi attinica situata soprattutto nel labbro inferiore con un'alta probabilità di trasformazione maligna.
Quali sono le cause?
Come dimostra chiaramente il nome, il principale fattore di insorgenza della cheratosi attinica è la luce solare. Infatti i raggi UV (UVB 280-320 nm) non solo danneggiano il DNA dei cheratinociti, ma diminuiscono anche la risposta immunitaria con riduzione della capacità di riparazione tissutale.
Come si sviluppa la malattia?
- Istologia: presenza di epidermide ispessita ed in parte atrofica con cheratinociti di dimensioni aumentate con paracheratosi ed atipie; nel derma sono presenti segni di degenerazione basofila del collagene (danno da raggi uv) ed infiltrato linfocitario;
- storia naturale: le cheratosi attiniche possono anche regredire spontaneamente, ma di solito permangono per anni; si stima che i carcinomi spinocellulari che insorgono su cheratosi attiniche in un anno siano 1/1000;
- diagnosi: clinicamente la cheratosi attinica esordisce con la comparsa di fini teleangectasie che nel tempo sono circondate da chiazze brune con sfumature rosate, sormontate da squame aderenti che possono essere rimosse con difficoltà; infatti, il distacco delle squame mostra una base eritematosa e causa un gemizio di sangue; alla palpazione le lesioni risultano essere ruvide; possono essere lesioni singole o multiple, inferiori al centimetro, a volte confluenti in larghe chiazze; i segni della trasformazione maligna sono rappresentati dall'indurimento e dall'ispessimento della lesione;
- terapia: il trattamento di elezione delle cheratosi attiniche è la crioterapia con azoto liquido. in caso di resistenza al trattamento o di recidiva è necessario asportare chirurgicamente la lesione. trattamenti topici con 5-fluorouracile topico, sodio diclofenac al 3% o applicazioni di acido tricloroacetico, sono utilizzati per pazienti inoperabili e per lesioni particolarmente estese e diffuse. tali trattamenti, solo parzialmente efficaci e possono determinare reazioni infiammatorie tali da dover sospendere la terapia.
Corno cutaneo
Un massivo accumulo di cheratina sopra una lesione epidermica, produce il corno cutaneo. La cheratosi attinica è la più frequente lesione precorritrice del corno cutaneo. Si localizza preferibilmente sulla rima del padiglione auricolare e sulla fronte. Può trasformarsi in carcinoma spinocellulare.
Leucoplachia
Chi è più colpito?
- Incidenza: Dipende da abitudini e tradizioni culturali. In Europa si riscontra in circa il 3% dei pazienti dermatologici.
- sesso: Il rapporto maschi: femmine è di 3:1; nei giovani 1:1.
- età: In genere si riscontra in soggetti adulti o anziani.
- sede anatomica: Mucosa orale (specie la zona mandibolare o geniena).
Quali sono le cause?
- Fumo e tabacco senza fumo;
- alcol;
- traumi;
- forse papillomavirus.
Come si ottiene una diagnosi?
È costituita da una lesione cheratosica del cavo orale, biancastra, di diametro superiore a 5 mm, che manovre di sfregamento non riescono ad asportare.È asintomatica, non ulcerata e non tende a sanguinare.
Come si sviluppa la malattia?
Istologicamente si osserva la presenza di alterazioni di tipo reattivo o di atipie. La cheratinizzazione di cellule isolate, l’atipia nucleare e le mitosi sono suggestive di trasformazione carcinomatosa in situ; il superamento della lamina propria può far porre diagnosi di spinalioma.
Le lesioni possono rimanere inalterate per anni estendendosi lentamente, ma nel 5% dei casi si possono trasformare in carcinoma. I fattori predittivi di tale trasformazione sono l'età della lesione (le più vecchie sono più pericolose), l'aspetto clinico non omogeneo (chiazze eritematose, erosioni e lesioni verrucose o papulari) e la localizzazione (pavimento della bocca, labbra e lingua).
Come si tratta?
La leucoplachia può essere tenuta in osservazione dopo rimozione delle eventuali cause evidenziate. Possono essere utili i retinoidi topici e per via orale, la crioterapia e la terapia con laser CO2. In casi appropriati, la lesione può essere escissa chirurgicamente.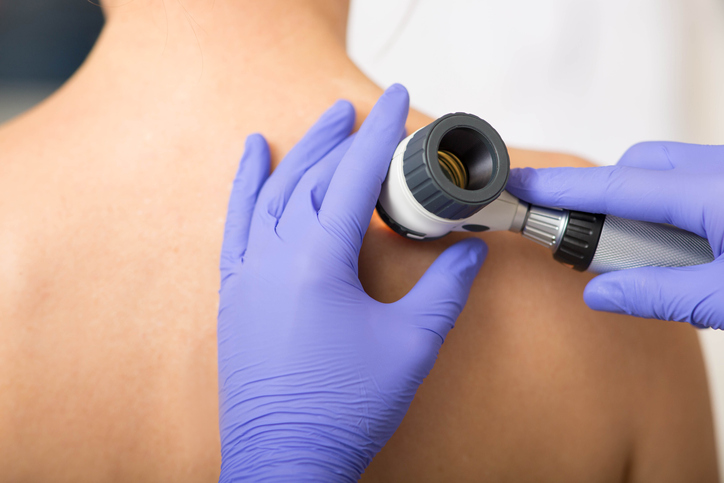
Morbo di Bowen
Si tratta di un epitelioma carcinoma squamocellulare in situ non correlato intraepidermico senza relazione con l'esposizione solare.
Chi è più colpito?
- Età: soprattutto in soggetti in età avanzata;
- sesso: sono colpiti in eguale misura i due sessi;
- etnia: soggetti di fototipo chiaro;
- sede anatomica: soprattutto localizzato su gambe e tronco.
Quali sono le cause?
In passato, l'insorgenza del morbo di Bowen era messa in relazione all'intossicazione da arsenico. Oggi è stato dimostrato che molte lesioni sono causate da infezione da HPV. Anche le radiazioni ionizzanti possono produrre lesioni bowenoidi.Come si sviluppa la malattia?
Le caratteristiche istologiche sono rappresentate da acantosi con ipercheratosi paracheratosica; perdita della disposizione a strati delle cellule dello strato spinoso; cellule grandi con nuclei voluminosi e pleomorfi; numerose mitosi; precoce cheratinizzazione di singole cellule; infiltrato dermico di cellule mononucleate e rare plasmacellule.La lesione può persistere per molti anni con una lentissima evoluzione che diventa francamente tumorale quando compaiono infiltrazione, noduli e ulcerazione.
Come si ottiene una diagnosi?
Il morbo di Bowen si presenta come una lesione solitaria, eritematosa, ovalare, non infiltrata, con bordo ben definito. La lesione è sormontata da squame e croste facilmente staccabili. La diagnosi è istologica.
Come si tratta?
Quando possibile, è sempre utile asportare chirurgicamente la lesione. In alternativa si possono utilizzare:- crioterapia;
- laserterapia CO2;
- trattamenti topici con 5-FU e imiquimod al 5%.
Eritroplasia di Queyrat
È la variante istotopomorfica del morbo di Bowen. Sedi elettive sono il glande, la lamina interna del prepuzio (quasi unicamente nei maschi non circoncisi) e l'interno delle piccole labbra. Sia il quadro istologico che l'evoluzione clinica si identificano con quelle del morbo di Bowen. È possibile la trasformazione in carcinoma con capacità di metastatizzare del 30% in più rispetto al morbo di Bowen.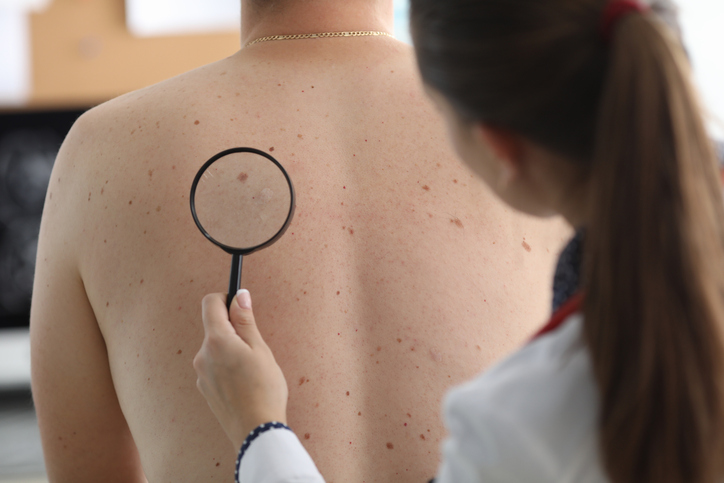
Epitelioma basocellulare
Chi è più colpito?
- Incidenza: gli epiteliomi basocellulari rappresentano da soli la metà di tutti i tumori maligni della pelle e costituiscono il cancro più diffuso dell’etnia bianca. Nell'ultimo decennio è stato rilevato un aumento dei casi in Europa, Australia e Stati Uniti, in questi ultimi con incidenza annuale di 150 casi ogni 100.000 abitanti;
- età: sono in genere colpiti soggetti in età più avanzata, ma è stato segnalato di recente un aumento di incidenza nei soggetti giovani;
- sesso: sono colpiti più gli uomini rispetto alle donne;
- etnia: notevolmente inferiore è l'incidenza nelle persone con pelle nera;
- sede anatomica: più frequentemente nelle zone esposte alla luce solare: terzo superiore del volto, regioni nasale, geniena, palpebrale, area temporale e frontale. Più raramente è interessato il tronco.
Quali sono le cause?
- Sindromi familiari: il carcinoma basocellulare si associa a numerose sindromi familiari: xeroderma pigmentosum, sindrome di gardner, sindrome di Jadassohn, sindrome di Torres, epidermodisplasia verruciforme, sindrome del nevo basocellulare, albinismo;
- caratteristiche fenotipiche: più colpiti sono i soggetti a cute chiara, con capelli biondi o rossi che si abbronzano al sole con difficoltà, con lentigginosi giovanile, soprattutto se vivono in alta quota o vicino all’equatore;
- radiazione solare: è implicata la radiazione uv, nella banda da 290 a 320 nm (UVB). La diminuzione dell’ozono atmosferico può contribuire ad aumentare il rischio di sviluppare la neoplasia;
- radiazioni ionizzanti: sono riportati carcinomi basocellulari in corrispondenza di radiodermiti secondarie a trattamento radiante;
- immunodepressione: il rischio di tumori cutanei aumenta in caso di immunosoppressione (AIDS, trapianto d'organi), la quale favorisce anche la fotocancerogenesi.
Biologia molecolare
Il ruolo dei raggi UV nella cancerogenesi degli epiteliomi è duplice. Essi provocano mutazioni a livello del DNA che, se non riparate, possono iniziare innescare il processo di trasformazione neoplastica. Inoltre, inducono alterazioni del sistema immunitario cutaneo, il quale non risulta in grado di reagire al danno indotto dalle contro le cellule tumorali. A livello molecolare, i tumori cutanei sono il risultato di una successione di alterazioni genetiche che modificano il processo di apoptosi dei cheratinociti danneggiati.La prima tappa nella carcinogenesi indotta dai raggi ultravioletti, soprattutto dagli UVB che hanno la capacità di penetrare parzialmente nello strato corneo con conseguente maggior assorbimento da parte del DNA, è la formazione di fotoprodotti del DNA (i più frequenti coinvolgono le pirimidine adiacenti quali i dimeri di ciclobutilpirimidina e il 6,4-pirimidin-pirimidone). Questi fotoprodotti, se non vengono eliminati dai sistemi di riparazione cellulare, (spesso alterati nei pazienti affetti da tali neoplasie), inducono lo sviluppo della neoplasia. A livello cellulare è presente l’attivazione di vari oncogeni: mutazione e amplificazione dei geni ras, importanti nel controllo delle prime fasi della cancerogenesi e soppressione di p53, normalmente deputato al controllo dell’apoptosi.
Inoltre, in vari studi sperimentali, è stato osservato un effetto immunosoppressivo indotto dalle radiazioni UV che, generalmente, determina soprattutto alterazioni della risposta cellulo-mediata. Tali effetti sono più difficili da individuare nell’uomo, ma sembra che le radiazioni UV provochino una cascata di eventi, con alterazione delle cellule APC (soprattutto delle cellule del Langherans) e della produzione di citochine (TNF, IL-10), che si traduce in un’alterata funzione del sistema immunitario che va a bloccare la reazione che l’organismo sviluppa in seguito al danno cutaneo da UV. un alterato funzionamento del sistema immunitario con conseguente mancata risposta dell’organismo al danno cutaneo indotto da UV.
Negli ultimi anni gli studi sulla patogenesi molecolare di questa neoplasia hanno aggiunto ulteriori ipotesi di cancerogenesi. Sia nelle forme sporadiche che in quelle familiari di carcinoma basocellulare, è stata riscontrata un’alterata attivazione del Sonic Hedgehog pathway (SHH, dimostratosi cruciale nello sviluppo dei vertebrati), mediata dal legame della proteina SHH con il PTCH1, gene oncosoppressore responsabile della sindrome di Gorlin-Goltz (mutazione della linea germinale) e le cui mutazioni sono state identificate nel 30-40 % delle forme sporadiche di epitelioma basocellulare. Studi su modelli transgenici di cute umana hanno confermato come l’attivazione dell’HH pathway risulti un evento precoce del processo di tumorigenesi.
Mutazioni del gene oncosoppressore p53 (implicato nel processo di apoptosi cellulare) sono state riscontrate in circa il 50% dei casi sporadici di neoplasia. Meno definita resta tuttora la relazione tra carcinoma basocellulare e mutazioni nella via del segnale dei geni RAS o RAF. Infine recentemente è stata dimostrata una correlazione tra la presenza di catenina nucleare ed un’aumentata proliferazione delle cellule tumorali. Argomento di grande interesse e studio dei giorni nostri è il ruolo dei microRNA nella patogenesi dei tumori cutanei epiteliali (miR-203 è stato recentemente associato alla morfogenesi cutanea e definito pertanto miRNA cute-specifico).
Come si sviluppa la malattia?
- Istologia: il tumore è costituito dalla presenza nel derma di cordoni di cellule epiteliali caratterizzate da grande nucleo ovalare intensamente basofilo e ridotto citoplasma, con scarse mitosi. Le travate sono disposte in maniera compatta ed appaiono delimitate da una palizzata di cellule cilindriche basofile simili alle cellule basali dell'epidermide. È caratteristica la neoformazione di stroma ricco di neo-fibroblasti e con presenza di degenerazione mucoide, fenomeno che non si osserva in nessun altro tumore di origine epiteliale. Si distinguono vari tipi morfologici e istologici tra cui la forma nodulare, superficiale, pigmentata e morfeica o sclerosante.
- storia naturale: il carcinoma basocellulare insorge sulle aree cutanee dotate di follicoli pilosebacei. Per quanto riguarda l'istogenesi, l'ipotesi attuale, derivata da studi immunoistochimici delle citocheratine, ne fa derivare l'origine dal follicolo pilosebaceo e precisamente dal rivestimento epiteliale esterno del follicolo, al di sotto dell'istmo. L'evoluzione è molto lenta e la malignità esclusivamente locale poiché i basaliomi non si accompagnano di norma a metastasi linfonodali o viscerali. Talora possono essere clinicamente aggressivi a causa della loro azione distruttiva sui tessuti profondi. Le metastasi sono rare e compaiono soprattutto quando le lesioni primarie sono di ampie dimensioni o nei soggetti anziani o immunodepressi. La sopravvivenza mediana dalla comparsa di metastasi è di 8 mesi.
Come si ottiene una diagnosi?
Clinicamente, il carcinoma basocellulare può avere aspetti quanto mai vari. Elementi diagnostici sono le cosiddette "perle epiteliali", la presenza di erosioni e/o di ulcerazioni che continuamente si riformano, ed inoltre l'età avanzata del paziente e la sede delle lesioni (due terzi superiori del volto). Si distinguono le seguenti forme clinico-evolutive:
- pagetoide: chiazza rosea con contorni arrotondati, con piccole squamo-croste su derma atrofico. piccole perle possono orlare la lesione;
- piano-cicatriziale: chiazza di forma irregolare, margini policiclici, atrofia centrale con presenza di perle translucide. può andare incontro ad ulcerazione;
- nodulare: piccole lesioni nodulari, lisce, a volte traslucide, solcate da teleangectasie, che lentamente aumentano di volume. sono di consistenza dura e tendono ad ombelicarsi e/o ulcerarsi al centro (fig. 59.2);
- pigmentato: può assumere lo stesso aspetto delle lesioni appena descritte, ma con intensa pigmentazione marrone-scuro o nera;
- ulcerato: ulcerazione profonda (ulcus rodens), non dolente, con base indurita, senza orletto perlaceo, l’evoluzione e la prognosi sono più gravi;
- terebrante: può rappresentare la fase avanzata delle forme precedenti o una neoplasia aggressiva fin dall’inizio che progredisce più in profondità con bordi infiltrati e a picco. il fondo è sanguinante e irregolare. è una forma destruente, mutilante e anche dolorosa.
Come si può prevenire?
Sebbene non esistano programmi di screening particolari, è raccomandato un esame annuale completo della cute. È importante, specie per il fototipo chiaro, evitare l'esposizione prolungata al sole nelle ore allo zenith nei mesi più caldi.
Come si tratta?
La terapia di scelta è chirurgica. La percentuale di recidive a 5 anni è in rapporto alle dimensioni del tumore e varia da circa il 3% per tumori <0.5 cm al 9% per tumori >1 cm. Nei tumori >2 cm, le recidive a 5 anni possono essere elevate. È importante controllare che i margini di resezione siano negativi. Nel caso di margini positivi, sono riportate recidive nel 40% dei pazienti entro 5 anni.
Dopo radioterapia, sono riportate percentuali di recidive a 5 anni in circa il 9% dei pazienti. Tali recidive, in genere, sono particolarmente distruttive e possono accompagnarsi a metastasi. La radioterapia è anche usata per il trattamento post-operatorio dei margini di resezione positivi.
Nei pazienti con tumori a rischio di recidiva, può essere usata la tecnica di Mohs (chirurgia micrografica) che consente di sterilizzare completamente l'area interessata. La crioterapia e la diatermocoagulazione possono dare risultati eccellenti se correttamente impiegate.
Per lesioni superficiali è in fase sperimentale la terapia fotodinamica Per lesioni superficiali trova da alcuni anni impiego la terapia fotodinamica e dal 2004 è in indicazione l’imiquimod al 5% in crema, imidazo-chinolina in grado di stimolare la risposta immunitaria locale promuovendo la produzione di citochine (IL-12, TNF e IFN). In casi selezionati, può essere usata la chemioterapia locale con 5-fluorouracile.
La chemioterapia sistemica è riservata ai casi con malattia locale non controllabile con altre modalità opzioni terapeutiche e con metastasi ovvero metastatica. Farmaci usati sono cisplatino, bleomicina, 5- fluorouracile, ciclofosfamide e vinblastina. Utile si è dimostrata l'associazione di cisplatino e doxorubicina.
Follow-up
Nei pazienti con tumori cutanei non melanomatosi, la frequenza dei controlli è in rapporto alla gravità della lesione trattata e al rischio di sviluppare un secondo tumore. Questo compare nel 20-30% dei pazienti entro 1 anno dal trattamento delle lesioni iniziali e nel 36% di essi entro il quinto anno. Controlli appropriati dovrebbero essere eseguiti ogni 6 mesi.
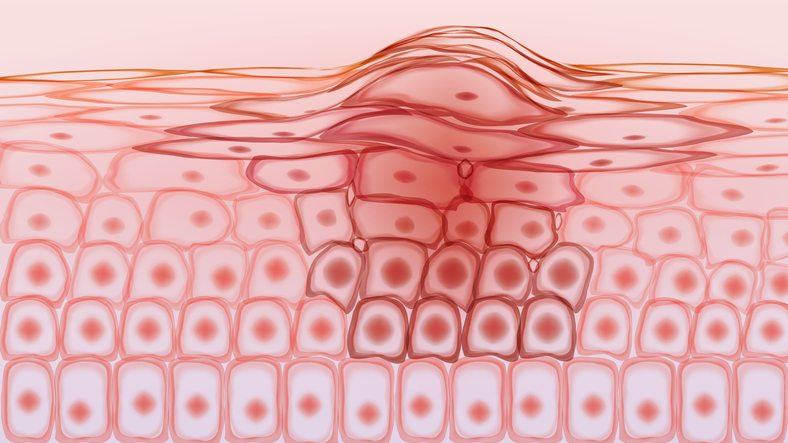
Sindrome del nevo basocellulare
È una sindrome ereditaria, denominata anche sindrome di Gorlin-Goltz, che coinvolge la cute con la comparsa di epiteliomi basocellulari, pits cornei palmoplantari e numerose anomalie in altri sistemi (ossa, tessuti molli, occhi, SNC, organi endocrini).
Chi è più colpito?
- Incidenza: anche se non ben conosciuta, la sindrome non è rara;
- età: comparsa dei primi epiteliomi in tarda infanzia;
- sesso: non vengono riportate differenze tra i due sessi;
- etnia: si osserva soprattutto nelle persone con pelle bianca, ma anche in quella afro-americana e nell'asiatica;
- sede: volto, collo, tronco e ascelle (con distribuzione bilaterale e simmetrica) con risparmio del cuoio capelluto e degli arti;
- eziologia: malattia ereditaria autosomica dominante a penetranza variabile. Il gene responsabile PTCH è localizzato sul cromosoma 9q22. Nelle aree fotoesposte compaiono più epiteliomi basocellulari.
Come si sviluppa la malattia?
Istologicamente i quadri comprendono tutti gli istotipi del basalioma:
- solido;
- adenoide;
- cistico;
- cheratosico; superficiale;
- fibroso.
Come si ottiene una diagnosi?
- Lesioni cutanee: epiteliomi nelle varie forme cliniche e pits cornei in sede palmoplantare;
- lesioni ossee: cisti mandibolari multiple, dentizione difettosa, spina bifida;
- lesioni oculari: strabismo, ipertelorismo, cecità congenita;
- lesioni del SNC: agenesia del corpo calloso, medulloblastoma;
- neoplasie interne: fibrosarcoma della mandibola, fibromi ovarici, teratomi e cistoadenomi.
Come si tratta?
Tutte le procedure descritte per il basalioma sono appropriate tranne la radioterapia, che tende ad indurre nuovi tumori nelle sedi irradiate.
Epitelioma squamocellulare
Chi è più colpito?
- Incidenza: è il secondo tumore maligno cutaneo più frequente. Il rapporto tra carcinoma basocellulare e spinocellulare varia tra 5:1 e 10:1 nella popolazione caucasica. Nelle persone con cute scura o nera il rapporto è più basso. I tumori cutanei non melanomatosi sono in costante aumento con un incremento annuale, negli USA, del 5.5% circa. L'incidenza è in rapporto alla latitudine (raddoppia ogni 8-10 gradi di avvicinamento all'equatore) e all'altitudine;
- sesso: più frequente nell'uomo rispetto alle donne (rapporto 2:1);
- età: più frequente nei soggetti anziani con un'incidenza 6 volte maggiore nei sessantenni rispetto ai quarantenni;
- etnia: piuttosto raro nelle persone con pelle nera, nella quale si osservano localizzazioni anche in aree non fotoesposte;
- sede anatomica: In circa il 75% dei casi si localizza al capo, elettivamente al terzo inferiore del volto, in particolare al labbro inferiore, attorno al naso e alla bocca. Altre localizzazioni sono: guance, tempie, orecchie, dorso delle mani, aree genitali.
Quali sono le cause?
- Sindromi familiari: elevata incidenza si osserva nello xeroderma pigmentosum, nell'epidermodisplasia verruciforme e nell'albinismo;
- caratteristiche fenotipiche: nei soggetti con cute chiara, esiste una evidente correlazione tra entità dell'esposizione solare e incidenza percentuale della neoplasia: Dopo esposizioni prolungate, sulla cute di zone fotoesposte di soggetti anziani si possono osservare lesioni multiple costituenti la cheratosi attinica, capace di evolvere in carcinoma squamoso;
- infezioni virali: sono chiamati in causa i papillomavirus. Questi virus sono importanti nella patogenesi della condilomatosi gigante di Buske-Löwernstein (HPV 6-11), nella epidermodisplasia verruciforme (HPV 5) e nel carcinoma cuniculatum;
- infiammazioni croniche: i carcinomi spinocellulari non insorgenti in zone cutanee esposte al sole, spesso insorgono in aree di flogosi croniche (cicatrici da ustione, fistole, ulcere da decubito, osteomielite cronica, lupus eritematoso discoide, granulomi cronici). Anche le cicatrici di vecchia data sono a rischio:
- Malattia di Bowen: è un carcinoma squamoso in situ che può insorgere in qualsiasi sede cutanea. Allorché localizzato sulla mucosa del glande, è detto eritroplasia di Queyrat. Nel corso di vari anni, entrambe le condizioni possono progredire verso un carcinoma squamoso invasivo con frequenza non elevata, maggiore per la eritroplasia di Queyrat.
- radiazioni: le radiazioni UVB costituiscono un fattore di rischio come per il basalioma e la diminuzione dell'ozono atmosferico aumenta l'esposizione a tale radiazione. La terapia PUVA (psoralene + UVA) impiegata nella psoriasi aumenta il rischio di carcinoma spinocellulare di 12 volte rispetto. Un altro fattore di rischio è costituito dalle radiodermiti. Di notevole interesse patogenetico è attualmente ritenuta la mutazione di p53 in seguito alla formazione di dimeri di ciclobutilpirimidina e di fotoprodotti (vedi epitelioma basocellulare Biologia molecolare). Nello studio della patogenesi molecolare di queste neoplasie si collocano il recente riscontro di un’iperespressione dell’EGFR nelle forme avanzate/metastatiche, un’iperespressione delle forme fosforilate di ATF2 (activating transcriptor factor-2) e STAT3 (signal transducer and activator of transcription-3), entrambi implicati nella trasduzione del segnale tumor-associata. Questi si sono infatti dimostrati overespressi in diverse casistiche di carcinomi squamocellulari cutanei, mostrando una correlazione inversa con il grado di differenziazione cellulare della neoplasia;
- immunodepressione: in tale condizione, il rischio di sviluppare un carcinoma spinocellulare è quasi il doppio rispetto al carcinoma basocellulare. Inoltre, questi tumori sono spesso più aggressivi e multipli;
- sostanze chimiche: sebbene oggi rappresentino un evento raro, carcinomi cutanei indotti da sostanze chimiche sono riportati in seguito ad esposizione professionale a fuliggine, paraffina, oli lubrificanti e idrocarburi o ingestione di quinacrina o arsenico (acqua, pesticidi).
Come si sviluppa la malattia?
- Istologia: si osserva una proliferazione anarchica di cellule malpighiane in evoluzione cheratinizzante. Le cellule sono atipiche, con ipercromia e iperplasia dei nuclei e numerose mitosi e con tendenza alla disposizione concentrica e progressiva cheratinizzazione verso il centro con formazione di globuli cornei. È costante la presenza di infiltrato infiammatorio;
- storia naturale: il carcinoma squamoso tende a diffondersi per estensione diretta e lungo gli spazi perineurali invadendo le strutture vicine. La diffusione per via linfatica è frequente, quella per via ematogena è rara (2-5%). Le metastasi a distanza si osservano più frequentemente a carico di: polmone, scheletro, fegato, cervello e reni. La maggior parte delle metastasi è evidenziata nei primi 2 anni e la sopravvivenza globale a 5 anni è intorno al 35%, indipendentemente dalla terapia.
Come si ottiene una diagnosi?
La biopsia è indicata per ogni lesione cutanea persistente. Forme clinico-evolutive:
- superficiale: chiazze poco infiltrate, di colore rosso-scuro, ricoperte da squamo-croste;
- vegetante: noduli o papillomi rosso-biancastri che possono raggiungere dimensioni considerevoli;
- nodulo-ulcerativo: nodulo più o meno rilevato, con base infiltrata e superficie irregolare. Rapidamente si ulcera assumendo l’aspetto di un cratere con fondo bianco-giallastro e piccole croste ematiche;
- cancroide: chiazza infiltrata con bordo netto. nella sua evoluzione diviene dapprima nodulare e poi ulcerato. è una forma particolarmente aggressiva e può rapidamente dare origine a metastasi (fig. 59.3).
Come si può prevenire?
Non esistono specifici programmi di screening, ma è raccomandato l'esame completo della cute una volta l'anno. Esami più frequenti (ogni 3-6 mesi) sono appropriati nei pazienti ad alto rischio (cheratosi attinica, malattia di Bowen, eritroplasia di Queyrat, xeroderma pigmentatum, cicatrici croniche da ustione, radiodermiti croniche, osteomieliti).
Stadiazione
È usata la classificazione TNM (Tabella 59.1). La classificazione si applica solo ai carcinomi, escludendo quelli della palpebra, della vulva e del pene. È necessario che ci sia la conferma istologica della neoplasia.
Qual è il decorso?
Sono noti vari fattori associati all'evoluzione dei carcinomi squamosi cutanei. La percentuale di recidive e di metastasi è minore per tumori di dimensioni <2 cm o con spessore <4 mm rispetto ai tumori con dimensioni o spessore maggiori. Gli istotipi con aspetto di cheratoacantoma hanno un decorso favorevole rispetto alla variante adenoide che ha prognosi cattiva. Più aggressivi sono i carcinomi a cellule fusate o indifferenziate. I tumori che si diffondono per via perineurale danno metastasi linfonodali e a distanza nel 35% e 15% dei casi contro, rispettivamente, il 15% e 3% dei tumori non dotati di neurotropismo. Un decorso più aggressivo è caratteristico dei tumori insorti su cicatrici o in ospiti immunocompromessi.
Come si tratta?
La terapia chirurgica costituisce il trattamento elettivo dei carcinomi squamosi cutanei, ponendo attenzione all'ottenimento di margini di resezione negativi. In caso di ricaduta, l'escissione chirurgica dà risultati inferiori con percentuali di recidive a 5 anni del 23%. Queste percentuali in caso di radioterapia primaria sono intorno al 10%. La radioterapia post-operatoria per tumori con margini di resezione positivi, riduce la probabilità di metastasi. Le percentuali più elevate di sopravvivenza a 5 anni sono ottenute con la tecnica di Mohs, indicata nei casi con lesioni >2 cm, bordi mal definiti, istologia aggressiva, interessamento perineurale, escissione incompleta o nei pazienti ad alto rischio. L'associazione di chirurgia e radioterapia è più efficace di ognuna delle due modalità usate singolarmente. La chemioterapia è indicata nei tumori localmente avanzati o metastatici, nei quali il regime più efficace è costituito dall'associazione di cisplatino e 5-fluorouracile.
Follow-up
Vedi carcinoma basocellulare.
Carcinoma a cellule di Merkel
Le cellule di Merkel furono inizialmente descritte, nel 1875, da Friedrich Sigmund Merkel che le denominò cellule tattili perché ritenute essere recettori tattili. Oggi sono generalmente interpretate come cellule originate dalla cresta neurale, riscontrabili come elementi singoli nella lamina basale dell’epidermide o raggruppate in modo da funzionare come recettori meccanici di tipo I. I primi casi di carcinoma a cellule di Merkel (CCM) furono descritti da Toker nel 1972. Finora in letteratura ne sono stati riportati circa 2000. Questo tumore è noto anche coi nomi di carcinoma neuroendocrino della cute o carcinoma a piccole cellule della cute.
Chi è più colpito?
- Incidenza: 0.23/100.000 in individui con pelle bianca e 0.01/100.000 con pelle nera. Negli Stati Uniti si stima che ogni anno si verifichino circa 470 nuovi casi di CCM. In alcune serie di pazienti è riportata una prevalenza nel sesso maschile, in altre in quello femminile;
- età: la media al momento della diagnosi è di 69 anni; solo il 5% dei pazienti ha un’età < 50 anni;
- sedi anatomiche: aree cutanee esposte al sole: faccia e collo (50%), estremità (40%), tronco e genitali (10%). Nel viso, spesso sono colpite le palpebre. Raramente il tumore insorge a carico della mucosa orale, vulva e pene;
Quali sono le cause?
L’esposizione solare e soprattutto la terapia PUVA sono considerati fattori di rischio, ma anche il danno da raggi infrarossi è stato chiamato in causa. Alcuni hanno riportato un ruolo patogenetico dell’esposizione all’arsenico. Un’altra possibile causa di CCM è la depressione immunitaria sia iatrogena (terapie immunosoppressive) che virale (HIV) o correlata alla presenza di una neoplasia. È riportata un’associazione con la leucemia linfatica cronica (11% dei casi) e con il carcinoma cheratinocitico, soprattutto quello squamocellulare.Tra le varie alterazioni cromosomiche riportate, la più importante sembra essere una delezione sul braccio corto del cromosoma 1 (1p36). Questa regione cromosomica è anche implicata nella patogenesi del retinoblastoma e del melanoma e si ritiene possa essere la sede di un gene oncosoppressore. In alcuni casi di CCM è espresso il gene p73 o, più frequentemente, il gene p53. È stata anche riportata una perdita di eterozigosi (LOH) a carico del cromosoma 3p21, una regione che è interessata anche in > 90% dei pazienti con carcinoma polmonare a piccole cellule. Ciò potrebbe indicare un pathway oncogeno comune per le due neoplasie. Altre alterazioni cromosomiche riportate sono:
- trisomia 1, 6, 11, 18;
- delezione del cromosoma 7;
- presenza di 2-3 copie del cromosoma X;
- LOH nel cromosoma 10q e 13.
Come si sviluppa la malattia?
- Istologia: la neoplasia è costituita da piccole cellule blu a bordi sfumati o indistinti, rotonde o poligonali, distribuite in modo da assumere aspetti di tipo solido, trabecolare o diffuso. La diagnosi differenziale va fatta soprattutto con PNET, carcinoma a piccole cellule metastatico, linfoma cutaneo e melanoma a piccole cellule e si basa sul profilo immunoistochimico. Questo, per il CCM, in genere è: CK20+, CK7-, NSE+, NFP+, S100-, LCA-, CD99+ (raramente), TTF1-;
- storia naturale: il tumore a cellule di Merkel origina nel derma e tende a diffondersi nel grasso sottocutaneo. Spesso l’epidermide è intatta, talora ulcerata. È una neoplasia a crescita rapida con tendenza a recidivare localmente ed a diffondersi ai linfonodi regionali. Frequenti sono anche le metastasi a distanza. Sedi di localizzazioni secondarie sono: cute (28%), linfonodi (27%), fegato (13%), polmone (10%), scheletro (10%), cervello (6%).
Stadiazione
Non esiste un sistema di stadiazione universalmente accettato per il CCM, ma spesso viene usato un sistema semplice proposto da Yiengpruksawan et al.:- stadio I, malattia cutanea localizzata (stadio IA 2 cm, IB > 2 cm);
- stadio II, malattia con interessamento linfonodale regionale;
- stadio III, malattia metastatica.
Come si ottiene una diagnosi?
Si presenta come un’unica lesione nodulare di diametro variabile da 0.5 a più di 10 cm, cupoliforme, di colore variabile da rosso-bruno a bluastro con superficie liscia e, a volte, con teleangectasie e ulcerazioni. I sintomi sono locali e correlati alla rapida crescita del tumore o all’interessamento linfonodale.
Dopo la diagnosi istologica, è necessario valutare l’estensione della malattia. Ciò in genere richiede una TC del torace, dell’addome e della pelvi ed una scintigrafia con octreotide marcato. Sempre più frequentemente viene usata la PET.
Qual è il decorso?
La maggior parte dei pazienti si presenta con malattia localizzata (70-80%); nel 10-30% dei casi esiste interessamento linfonodale e nell’1-4% sono presenti metastasi a distanza al momento della diagnosi. Fattori prognostici favorevoli sono considerati: sede primaria a carico del viso e del collo e assenza di metastasi linfonodali, stadio IA, sesso femminile. Inizialmente considerato un tumore a prognosi favorevole, il CCM è oggi ritenuto una neoplasia altamente aggressiva e letale. Ricadute sono riportate nel 55-79% dei casi, spesso locali o linfonodali, con comparsa generalmente 6-12 mesi dopo la diagnosi iniziale.Come si tratta?
Considerata la rarità del CCM, non esistono studi prospettici che abbiano valutato l’efficacia delle singole modalità terapeutiche in uso in questa neoplasia. Tuttavia, alcune linee-guida generali possono essere suggerite.Nella malattia localizzata è indicata l’escissione chirurgica ampia con margini di resezione negativi. In genere sono raccomandati margini di resezione di 2-3 cm con una profondità di 2 cm. La chirurgia micrografica secondo Mohs è stata proposta soprattutto in zone cosmeticamente importanti, quali il viso.
Un interessamento linfonodale regionale è presente nel 10-30% dei pazienti sottoposti a linfadenectomia.
Pertanto, una dissezione linfonodale elettiva è stata raccomandata soprattutto in pazienti giovani con tumori voluminosi. In considerazione della similarità tra CCM e melanoma per quanto riguarda le modalità di diffusione, si è osservato un ricorso sempre più frequente alla tecnica del linfonodo sentinella. Allo stato attuale, tuttavia, non si possono trarre conclusioni definitive sulla reale utilità della linfoadenectomia nel prevenire le ricadute regionali.
Considerata la somiglianza col carcinoma polmonare a piccole cellule, il CCM è stato spesso trattato con radioterapia e vari studi hanno evidenziato che questa modalità terapeutica può essere di beneficio sia come trattamento adiuvante che nella malattia in fase avanzata. In genere, si ritiene che la somministrazione di 40-50 Gy sulla sede primaria e sui linfonodi interessati dopo l’intervento chirurgico, possa essere di beneficio nel prevenire le recidive locali.
Vari studi hanno riportato buoni risultati con regimi di chemioterapia simili a quelli in uso nel carcinoma polmonare a piccole cellule. Generalmente, la percentuale di risposte globali è stata del 60-70% con associazioni più spesso comprendenti ciclofosfamide, antracicline, cisplatino e fluorouracile. Attualmente, la chemioterapia non ha un ruolo definitivo come terapia adiuvante, ma trova indicazione nella malattia metastatica. Regimi di uso frequente sono FEC, FAC, PE, CAV. Non c’è ancora esperienza con i taxani che pur potrebbero essere usati nel CCM.
Occasionalmente si è fatto ricorso all’uso di interferone e tumor necrosis factor. IFN è stato somministrato come agente singolo o in associazione alla chemioterapia, ma non esiste evidenza sicura che possa essere di beneficio. Il TNF è stato usato per via intralesionale con regressione completa della lesione. La presenza di recettori per la somatostatina nel CCM ha indotto anche ad usare l'octreotide.
L’acido farnesiltiosalicilico, un inibitore della ras pathway, è risultato in grado di inibire la crescita di CCM in topi SCID. Nelle cellule CCM è spesso iperespresso bcl-2 ed oligonucleotidi antisenso anti-bcl-2 hanno determinato l’inibizione di queste cellule in topi SCID. Questi studi iniziali possono far sperare che nel futuro potranno essere disponibili farmaci a bersaglio molecolare efficaci nella terapia del carcinoma a cellule di Merkel.
Tumori degli annessi cutanei
Tra i tumori degli annessi cutanei si possono distinguere forme benigne, relativamente frequenti e legate all'età giovanile, e forme maligne, molto più rare, che possono comparire in tutte le età. Nella maggior parte dei casi si presentano come una lesione nodulare unica, dello stesso colore della cute o di color rosso, frequentemente al capo.
Tali caratteristiche, simili ai nevi melanocitari dermici, alle cisti epidermoidi e al carcinoma basocellulare, non permettono quasi mai una diagnosi clinica che invece viene quasi sempre posta a livello istologico. I tumori possono originare dal follicolo pilifero, dalle ghiandole eccrine, apocrine e sebacee. Spesso è difficile determinare la reale origine del tumore ed è per questo che si pensa possano prendere origine da cellule epiteliali più primitive che successivamente si differenziano in una struttura annessiale.
Carcinoma annessiale microcistico
Il carcinoma annessiale microcistico (CAM) fu inizialmente descritto da Goldstein et al. nel 1982 come tumore a lenta crescita con aspetti di differenziazione follicolare, apocrina, eccrina, sebacea e di dotti sudoripari. Per questo è stato anche denominato tumore annessiale combinato, carcinoma sclerosante dei dotti sudoripari, carcinoma siringomatoso (ben differenziato) e siringoma maligno, ad indicare l’origine dalle ghiandole sudoripare e la somiglianza col siringoma benigno.
È un tumore dell’età avanzata (età media circa 63 anni) che si osserva prevalentemente nel sesso femminile. Fattori di rischio sono considerati le radiazioni ionizzanti (spesso il tumore si riscontra vicino ad aree irradiate) e quelle ultraviolette. Probabilmente hanno un ruolo anche fattori genetici. La sede preferita è la testa e il collo, soprattutto nelle zone periorale e perioculare e a livello del cuoio capelluto. Rara è la sede ascellare.
Generalmente si presenta come nodulo solitario o placca di colore roseo-rosso, di consistenza dura, con margini indistinti, talora di aspetto cistico. Distendendo la cute sovrastante il nodulo può osservarsi un colore giallastro. Il tumore ha un comportamento aggressivo locale e può infiltrare le strutture sottostanti, ma le metastasi sono estremamente rare. In pazienti immunocompromessi sono state riportate metastasi in transito e linfonodali.
Istologicamente il tumore in genere non presenta connessioni con l’epidermide. Il derma è infiltrato da nidi e cordoni di cheratinociti con due componenti classiche, piccoli dotti e strutture cistiche. Poiché il tumore ha margini mal definiti e profondi e tende a diffondersi per via perineurale, l’asportazione chirurgica deve essere ampia e preferenzialmente eseguita con la tecnica di Mohs. La percentuale di recidive locali è elevata con comparsa talora dopo molti anni dal trattamento iniziale.
Il CAM è considerato un tumore radioresistente, ma la radioterapia può essere talora di beneficio nell’alleviare i sintomi. Alcuni consigliano l’uso della radioterapia postoperatoria in caso di invasione perineurale o delle strutture profonde o di margini di resezione positivi.
Porocarcinoma
È il tumore più frequente tra quelli annessiali, si riscontra in genere in pazienti anziani ed ha sede preferibilmente agli arti inferiori (44%), al tronco (24%) ed al capo (18%). Talora la neoplasia è diagnosticata come carcinoma in situ. Allorché diventa invasiva, tende ad infiltrare il derma similmente al carcinoma spinocellulare.La differenziazione duttale è la caratteristica più significativa. Non sempre è agevole identificare la struttura eccrina e apocrina del tumore. La terapia è costituita dalla escissione chirurgica. Recidive locali si osservano in circa il 17% dei casi, metastasi linfonodali nel 19% ed a distanza nell’11% dei pazienti. Fattori prognostici indicativi di particolare aggressività sono: numero di mitosi > 14 per HPF, invasione linfovascolare, spessore > 7 mm.
Carcinoma sebaceo
Rappresenta lo 0.2% dei tumori cutanei e si presenta in età avanzata (età media: 65 anni) con prevalenza nel sesso maschile. Nel 50% dei casi è localizzato alle palpebre, mentre il restante 50% si riscontra nelle zone dove sono presenti ghiandole sebacee.
L’aspetto è di un nodulo o una placca solitari, di colore giallo o arancione, più o meno traslucidi e ricoperti da cute normale o lievemente verrucosa. La crescita è molto lenta e rare sono le metastasi. La neoplasia può presentarsi come carcinoma in situ con voluminose cellule chiare similmente al melanoma in situ o al morbo di Paget o alla malattia di Bowen. La terapia consiste nella escissione chirurgica completa.

Tumori cutanei metastatici
Le metastasi cutanee di neoplasie primitive di altri organi sono di rilievo ai fini prognostici (in senso negativo) e diagnostici, in quanto spesso epifenomeno di neoplasie misconosciute. La via di metastatizzazione è prevalentemente linfatica (mammella e cavo orale) o ematica (altri carcinomi).
Chi è più colpito?
Incidenza: dall’1% al 10% dei pazienti oncologici;
età: soggetti adulti o anziani;
sesso: la frequenza dei tumori primitivi varia con il sesso;
sedi anatomiche: femmine: mammella (70%), intestino (8%), melanoma (5%), polmone (4%), ovaio (4%), sarcoma (2%),cervice (2%), pancreas (2%), scc del cavo orale (1%), vescica (1%); maschi: polmone (24%), intestino (20%), melanoma (13%), scc del cavo orale (12%), rene (6%), stomaco (6%), vescica (6%), mammella (2%), prostata (1%), scc cutaneo (1%).
Come si sviluppa la malattia?
All’esame obiettivo le lesioni cutanee possono presentarsi sotto forma di nodulo, placca rilevata, area fibrosa ispessita. Si scoprono quando superano i 5 mm e la diagnosi di certezza è sempre istologica. L’area fibrosa può mimare la morfea e al cuoio capelluto può causare alopecia.
Inizialmente l’epidermide è integra e tesa sul nodulo, ma con l’andar del tempo la superficie può ulcerarsi e diventare ipercheratosica. Il colore varia dal rosa al rosso nelle manifestazioni infiammatorie, mentre in caso di secondarismi cutanei da melanoma i noduli dermici saranno di colore blu-grigio-nero. Ogni neoplasia primitiva presenta diversi pattern di interessamento cutaneo che, a seconda dell’estensione e della regione interessata, identificano determinate varianti cliniche.
Carcinoma della mammella
- Carcinoma en cuirasse o scirroso: di solito estensione locale di un tumore mammario in regione presternale, si presenta come una placca irregolare e dura che genera successivamente un indurimento cutaneo diffuso, simile alla morfea. Esordisce con papule e noduli sparsi, lenticolari, a superficie liscia eritematosa o rosso-blu; quest’ultimi si riuniscono quindi a formare una placca sclerodermiforme, senza alcuna infiammazione associata. Compare anche con neoplasie primitive del polmone, del tratto GI e del rene;
- malattia di Paget: estensione epidermica, in regione areolare, di una neoplasia mammaria sottostante; simile ad una chiazza eczematosa, eritematosa e desquamativa o dall’aspetto a placca nettamente delimitata;
- carcinoma infiammatorio o erisipeloide: si presenta come una chiazza o placca unica, eritematosa, calda e con bordo in espansione. È abitualmente a primitività mammaria, ma può comparire anche con altri primitivi (pancreas, parotide, tonsille, colon, stomaco, retto, melanoma, ovaio, utero, prostata, polmone);
- carcinoma teleangectasico: tumore mammario caratterizzato da teleangectasie a capocchia di spillo, con capillari dilatati e presenza di papulo-vescicole multiple, dal colorito violaceo, simile a quello del linfangioma circoscritto;
- nodulo di Suor Mary Joseph: lesione metastatica all’ombelico, derivante da una neoplasia intraaddominale (stomaco, colon, ovaio e pancreas); raramente il primitivo può essere mammario. Più facilmente obiettivabile con la palpazione che con l’ispezione, può presentarsi come nodulo/i solido e duro, di aspetto vascolare, fissurato, ulcerato o suppurato;
- alopecia neoplastica: compare per diffusione ematogena. Il cuoio capelluto presenta aree prive di capelli ben delimitate, a superficie liscia e dal colorito rosso-rosa, in un quadro sovrapponibile a quello dell’alopecia areata;
- carcinoma intestinale: spesso si manifesta sulla cute dell’addome o del perineo, ovvero capillizio e volto. La maggior parte origina dal retto. Può manifestarsi come un carcinoma metastatico infiammatorio della regione inguinale, dell’area sopraclavicolare oppure del volto e del collo;
- carcinoma del polmone: può indurre la formazione di un gran numero di noduli metastatici in poco tempo. Più frequentemente si tratta di noduli rossastri su tronco/cuoio capelluto, simmetrici, lungo la direzione dei vasi intercostali (può essere zosteriforme) ovvero a livello della cicatrice (in sede di toracotomia);
- melanoma: attraverso i linfatici può diffondersi in una sede cutanea a distanza da quella primitiva. Sedi d’origine possono essere anche altre non cutanee: occhi, cervice, cavo orale. Abitualmente si tratta di noduli singoli o multipli, iperpigmentati, spesso a seguire il decorso dei linfatici (metastasi in transit);
- carcinoma della vescica e dell’ovaio: possono diffondersi per contiguità alla cute addominale ed inguinale in modo analogo al carcinoma mammario, con caratteristiche simili all’erisipela.
Diagnosi e terapia
Come già enunciato, la diagnosi di certezza è sempre istologica. Recenti studi incentrati sulla diagnosi dermoscopica delle micrometastasi cutanee di melanoma (caratterizzate da pattern sacculare, aspetto “aneurismatico” e tortuosità dei vasi, alone eritematoso e/o pigmentario) hanno consentito una corretta diagnosi differenziale delle stesse con altre lesioni nodulari cutanee benigne, melanomi nodulari e basaliomi nodulo-cistici.In caso di lesione singola o in numero limitato può essere indicata l'asportazione chirurgica, restando cardine del momento terapeutico il trattamento sistemico della neoplasia primitiva.
Bibliografia
- Albert MR, Weinstock MA: Keratinocyte carcinoma. CA Cancer J Clin 53: 292-302, 2003.
- Bale AE: The nevoid basal cell carcinoma syndrome: genetics and mechanism of carcinogenesis. Cancer Invest 15: 180-186, 1997.
- Braun-Falco O, Plawig G, Wolff HH: Burgdorf WHC. Dermatology. Springer-Verlag Berlin Heidelberg 2000.
- Friedman PM, Friedman RH, Jiang SB, et al.: Microcystic adnexal carcinoma: collaborative series review and update. J Am Acad Dermatol 41: 225-231, 1999
- Goessling W, McKee PH, Mayer RJ: Merkel cell carcinoma. J Clin Oncol 20: 588-598, 2002.
- Grossman D, Leffell DJ: The molecular basis of non-melanoma skin cancer: new understanding. Arch Dermatol 133: 1263-1270, 1997.
- Lawrence CM: Mohs' micrographic surgery for basal cell carcinoma. Clin Exp Dermatol 24: 130-133, 1999.
- Menzies SW: Dermoscopy of pigmented basal cell carcinoma. Clinics in Dermatology. 220: 268-269, 2002.
- Nelson BR, Hamlet KR, Gillard M, et al.: Sebaceous carcinoma. J Am Acad Dermatol 33: 1-15, 1995.
- Ongenae KC, Verhaegh MEJM, Vermeulen AHM, et al.: Microcystic adnexal carcinoma: An uncommon tumor with debatable origin. Dermatol Surg 27: 979-984, 2001.
- Plunkett TA, Harris AJ, Ogg CS et al. The treatment of Merkel cell carcinoma and its association with immunosoppression. Br J Dermatol 139: 345, 1998
- Robson A, Green J, Ansari N, et al.: Eccrine porocarcinoma (Malignant Eccrine Poroma). Am J Surg Pathol 25: 710-720, 2001
- Schwartz RA. Premalignant Keratinocytic neoplasm. J Am Acad Dermatol 35: 223-242, 1996
- Shin DM: Paclitaxel (Taxol)/ifosfamide-based chemotherapy in patients with recurrent or metastatic squamous cell carcinoma of the head and neck. Semin Oncol 27: 36-40, 2000
- Thissen Mr, Neumann MH, Schouten LJ: A systematic rewiev of treatment modalities for primary basal cell carcinomas. Arch Dermatol 135: 1177-1183, 1999
- Woodhead AD, Setlow RB, Tanaka M: Environmental factors in non-melanoma and melanoma skin cancer. J Epidemiol 9: S102-S104, 1999
- Epstein EH. Basal cell carcinomas: attack of the hedgehog. Nature Reviews Cancer 2008; 8: 743-54.
- Mariwalla K, Aasi SZ, Glusac EJ, et al. Mohs micrographic surgery histopathology concordance. J Am Acad Dermatol 2009; 60: 94-8.
- Rubin AI, Chen EH, Ratner D. Basal-Cell Carcinoma. N Engl J Med 2005; 353: 2262-9.
- Garcia C, Poletti E, Crowson N. Basosquamous carcinoma. J Am Acad Dermatol 2009; 60: 137-43.
- Sand M, Gambichler T, Sand D, et al. MicroRNAs and the skin: tiny players in the body’s largest organ. J Dermatol Sci 2009; 53: 169-75.
- Alam M, Ratner D. Cutaneous Squamous-Cell Carcinoma. N Engl J Med 2001; 344: 975-83.
- Chen S, Takeuchi S. Overexpression of phosphorylated-ATF2 and STAT3 in cutaneous squamous cell carcinoma, Bowen’s disease and basal cell carcinoma. J Derm Sci 2008; 51: 210-5 (Editorial).
- Van der Geer S, Ostertag JU, Krekels GAM. Treatment of basal cell carcinoma in patients with nevoid basal cell carcinoma syndrome. JEADV 2009; 23: 308-13.
- Karve SJ, Feldman SR, Yentzer BA, et al. Imiquimod: a review of basal cell carcinoma treatments. J Drugs Dermatol 2008; 7(11): 1044-51.
- Bono R, Giampetruzzi AR, Concolino F, et al. Dermoscopic paterns of cutaneos melanoma metastases. Melanoma Res 2004; 14: 367-73.


